化学基礎課題プリント28より
化学基礎課題プリント28より
4節 酸化還元反応の応用
A.電池のしくみ
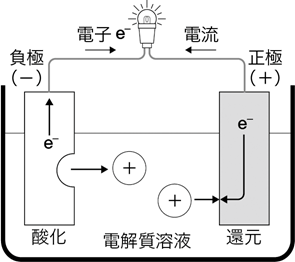
酸化還元反応を利用して,電気エネルギーを取り出す装置を( 電池(化学電池) )という。
イオン化傾向の異なる金属を電解質水溶液に浸して導線で結ぶと電流が流れる。
・イオン化傾向の( 大きな )金属…( 酸化 )反応が起こり,陽イオンになる。
・イオン化傾向の( 小さな )金属…電子が流れ込み,( 還元 )反応が起こる。
電池において,水溶液に浸した物質を( 電極 )という。
・( 酸化 )反応が起こって電子が流れ出す電極
…( 負極 )
・電子が流れ込んで( 還元 )反応が起こる電極
…( 正極 )
両電極の間に生じる電位差を電池の( 起電力 )という。
なお,( 電子 )は負極 → 正極へ流れ,( 電流 )は正極 → 負極へ流れる。
B.実用電池
電池から電流を取り出すこと。 … ( 放電 )
放電と逆向きに電流を流し,起電力を回復させる操作。 … ( 充電 )
充電できず起電力が回復できない電池。 … ( 一次電池 )
充電により起電力が回復できる電池。 … ( 二次電池(蓄電池) )
水素と酸素から水ができる化学反応を利用した電池。 … ( 燃料電池 )
D.酸化剤と還元剤の量的関係
還元剤が放出する電子の数と酸化剤が受け取る電子の数が等しいとき,酸化剤と還元剤は過不足なく反応する。この量的関係を利用すると,濃度が正確にわかっている酸化剤(または還元剤)を用いて,濃度がわからない還元剤(または酸化剤)の濃度を求めることができる。このような操作を(酸化還元滴定)といい,器具と操作方法は中和滴定とほぼ同じである。
濃度 × 体積 × e-の係数 = 濃度 × 体積 × e-の係数
インプレスの問題をやってみよう。
244 塩素と硫酸鉄(Ⅱ)がそれぞれ酸化剤,還元剤として働くとき,電子の授受を表す式は次の①,②のようになる。 Cl2+2e-→2Cl-…① Fe2+→Fe3++e-…②
0.1mol/Lの硫酸鉄(Ⅱ)水溶液100mLを完全に酸化するには,0.1mol/Lの塩素水が少なくとも何mL必要か。
0.1 × 100/1000 × 1 = 0.1 × x/1000 × 2
100 = 2x x=50